Hlava 21 Část 11 Sbírky federálních nařízení (Code of Federal Regulations – CFR) definuje kritéria pro integritu elektronických dat tak, jak jsou stanovena americkým Úřadem pro kontrolu potravin a léčiv (FDA). K zajištění přesných elektronických záznamů a podpisů musí odvětví regulovaná úřadem FDA, jako jsou výrobci zdravotnických prostředků a léčiv, splnit požadavky uvedené ve směrnici21 CFR Part 11.
Dodržování těchto požadavků však může být těžké a časově náročné. Tento blog se zaměří na obvyklé problémy spojené s dodržováním směrnice 21 CFR Part 11 a představí způsoby, jak řešení těchto problémů usnadnit.
Problémy při dodržování shody se směrnicí 21 CFR Part 11
Shoda zpravidla zahrnuje vytvoření pracovních pokynů pro splnění každého konkrétního nařízení směrnice 21 CFR Part 11, vypracování validačních protokolů pro zajištění správného nastavení, provozu a funkce zařízení a softwaru, vytvoření standardních pracovních postupů (Standard Operating Procedures – SOP) a rozsáhlé školení pracovníků, kteří používají daná zařízení a software.
Každý nástroj, který tento proces usnadní, je užitečný.
Mnoho výrobců, kteří působí v odvětvích regulovaných úřadem FDA, používají náš systém kontroly technické čistotyOLYMPUS CIX100. Systém CIX100 s možnostmi intuitivního rozhraní, efektivního sběru dat a rychlého podávání zpráv vám může pomoci rychle a snadno zhodnotit čistotu vyráběných součástí, abyste zjistili, zda tyto součásti splňují standardy společnosti a mezinárodní normy.
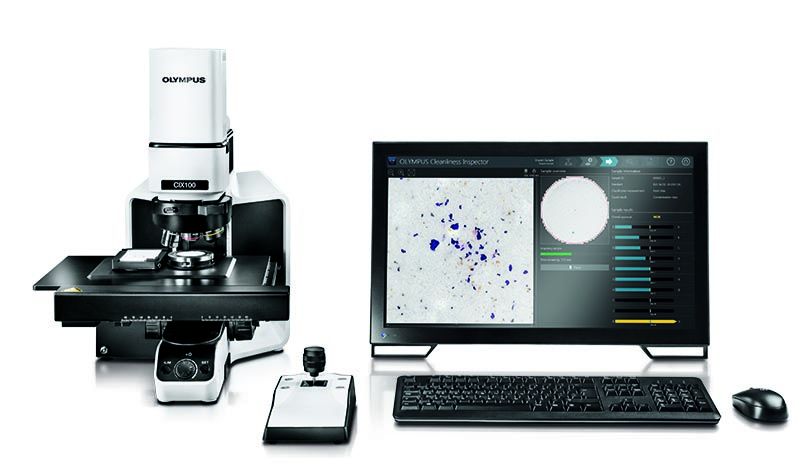
Systém kontroly čistoty OLYMPUS CIX100
Abychom vám usnadnili splnění těchto požadavků, vytvořili jsme pro systém kontroly čistoty CIX100 balíček 21 CFR Part 11.
Zjednodušení shody se směrnicí 21 CFR Part 11 pomocí systému kontroly čistoty CIX100.
Náš balíček CIX100 21 CFR Part 11 ukazuje, jak je možné s pomocí systému CIX100 zajistit shodu s každým požadavkem, a představuje dokumenty pro nastavení systému a provozu. Pokud balíček správně implementujete, splní systém CIX100 požadavky směrnice 21 CFR Part 11.
Balíček obsahuje:
- dokumentaci, která popisuje, jak systém CIX100 s pomocí služby Adobe Sign splní konkrétní požadavky směrnice 21 CFR Part 11.
- CIX100 validační protokol pro instalační kvalifikaci / operační kvalifikaci (IQ/OQ)
- standardní pracovní postupy (SOP) pro systém CIX100 v souladu se směrnicí 21 CFR Part 11
- pracovní pokyny pro nastavení a provoz systému CIX100 v souladu se směrnicí 21 CFR Part 11
Postup shody se směrnicí 21 CFR Part 11
Pomocí těchto podrobných zdrojů balíček jasně popisuje to, co potřebujete vědět ke splnění požadavků směrnice 21 CFR Part 11. Tj. jaká řešení poskytujeme a případné zbývající odpovědnosti uživatele. Rychlý přehled:
Řešení předpisů směrnice 21 CFR Part 11 společnosti Olympus zahrnuje:
- validaci systému pro přesné a spolehlivé výsledky prostřednictvím IQ/OQ
- zajištění školení CIX100 pro uživatele mikroskopu
- zajištění správného provozu prostřednictvím detailních standardních pracovních postupů
- omezení přístupu k systému pouze pro oprávněné osoby pomocí přihlášení do Windows PC a správy práv uživatele
- použití služby Adobe Sign k zajištění elektronických podpisů a sledování PDF zpráv z kontrol vzorků
Odpovědnosti uživatele zahrnují:
- zajištění školení Adobe Sign pro elektronické podpisy a sledování elektronických dat
- vytváření strategií pro používání softwaru CIX100 pomocí služby Adobe Sign a sledování přístupu a revizí předchozích zpráv z kontrol vzorků
- zavedení postupů pro loss management a uchovávání dokladů
S tímto balíčkem vám pomůže systém CIX100 zefektivnit kontroly čistoty a splnit požadavky těchto důležitých standardů úřadu FDA, jež jsou kladeny na elektronické záznamy a podpisy.
Související obsah
Úvod do kontroly technické čistoty
Pět způsobů, kterými systém kontroly čistoty OLYMPUS CIX100 poskytuje reprodukovatelné výsledky
Prospekt: vysvětlení standardů technické čistoty
Kontaktujte nás

