O Título 21, Parte 11, do Código de Regulamentações Federais (CFR) define os critérios para integridade de dados eletrônicos conforme estabelecido pela Food and Drug Administration (FDA) dos Estados Unidos. Indústrias regulamentadas pela FDA, como fabricantes de dispositivos médicos e empresas farmacêuticas, devem cumprir o CFR 21 Parte 11 para garantir registros e assinaturas eletrônicas precisas.
No entanto, cumprir esses requisitos pode ser difícil e demorado. Este blog explorará os desafios comuns de cumprir a CFR 21 Parte 11 e discutirá maneiras de amenizá-los.
Os desafios do cumprimento da CFR 21 Parte 11
A conformidade normalmente envolve a criação de instruções de trabalho para atender a cada regulamento específico da CFR 21 Parte 11, o desenvolvimento de protocolos de validação para garantir a configuração, operação e desempenho adequados de equipamentos e software, criação de procedimentos operacionais padrão (SOP) e treinamento extensivo para o pessoal que usa o equipamento e programas.
Qualquer ferramenta que facilite esse processo é útil.
Muitos fabricantes em setores regulamentados pelo FDA usam nosso inspetor de limpeza técnica OLYMPUS CIX100. Construído com uma interface intuitiva, aquisição de dados eficiente e opções de relatórios rápidos, o sistema CIX100 pode ajudá-lo a avaliar de forma rápida e fácil a limpeza dos componentes fabricados para determinar se eles estão de acordo com os padrões da empresa e internacionais.
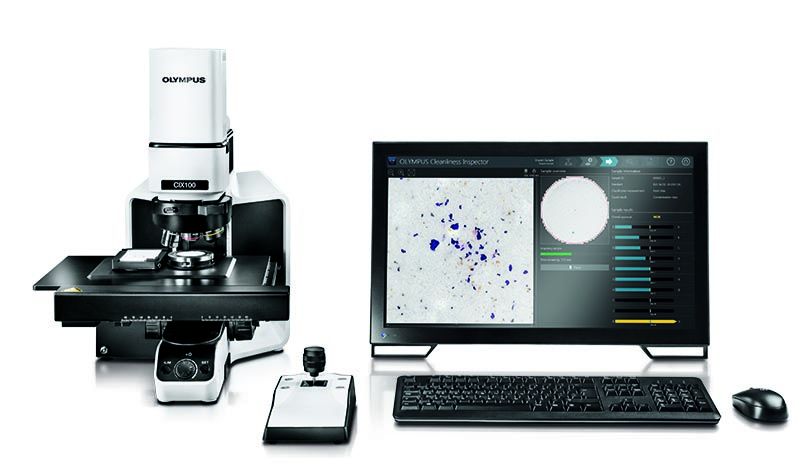
O inspetor de limpeza OLYMPUS CIX100.
Para ajudá-lo a cumprir facilmente esses requisitos, criamos um pacote CFR 21 Parte 11 para o inspetor de limpeza CIX100.
Simplificando a conformidade CFR 21 Parte 11 usando o Inspetor de Limpeza CIX100
Nosso pacote CIX100 CFR 21 Parte 11 demonstra como o sistema CIX100 pode cumprir a conformidade de cada requisito e fornece documentos para configuração e operação do sistema. Quando o pacote é implementado corretamente, o sistema CIX100 está em conformidade com a CFR 21 Parte 11.
O pacote inclui:
- Documentos detalhando como o sistema CIX100 com Adobe Sign atende aos requisitos específicos da CFR 21 Parte 11
- Protocolo de validação CIX100 para qualificação de instalação/qualificação operacional (IQ/OQ)
- Procedimento operacional padrão (SOP) para o sistema CIX100 em conformidade com a CFR 21 Parte 11
- Instruções de trabalho para a configuração e operação do sistema CIX100 em conformidade com a CFR 21 Parte 11
Roteiro para a conformidade CFR 21 Parte 11
Com esses recursos detalhados, o pacote apresenta claramente o que você precisa saber para atender aos requisitos da CFR 21 Parte 11. Isso inclui as soluções que oferecemos e quaisquer responsabilidades restantes do usuário. Esta é uma visão geral rápida:
As soluções da Olympus para as conformidades CFR 21 Parte 11 incluem:
- Validar o sistema para resultados precisos e confiáveis por meio de IQ/OQ
- Oferecer treinamento do CIX100 para usuários de microscópio
- Garantir a operação adequada com um SOP detalhado
- Restringir o acesso do sistema a indivíduos autorizados por meio de um login de PC com Windows e gerenciamento de direitos de usuário
- Usar o Adobe Sign para fornecer assinaturas eletrônicas e rastrear relatórios em PDF de inspeções de amostra
As responsabilidades do usuário incluem:
- Fornecer treinamento para o Adobe Sign para assinaturas eletrônicas e rastreamento de dados eletrônicos
- Criar políticas para usar o software CIX100 com Adobe Sign e para rastrear o acesso e as revisões de relatórios de inspeção de amostra anteriores
- Manter procedimentos para gestão de perdas e retenção de documentos
Com este pacote, o sistema CIX100 pode ajudá-lo a agilizar as inspeções de limpeza e atender a conformidade com esses importantes padrões do FDA para registros e assinaturas eletrônicas.
Conteúdo relacionado
Introdução à inspeção de limpeza técnica
Cinco maneiras de o inspetor de limpeza OLYMPUS CIX100 fornecer resultados reproduzíveis
Brochura: Explicação das normas de limpeza técnica
Entre em contato

